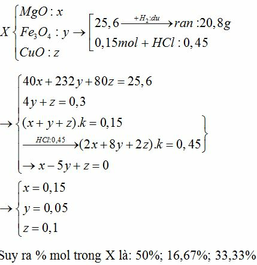Cho một lượng CO dư đi qua 25,6 hỗn hợp X gồm Fe3O4 , MgO và CuO , thu được 20,8 g chất rắn . Cho 450 ml HCl 2M phản ứng với 25,6 g hỗn hợp X
a , viết tất cả ptpu có thể xảy ra
b, tính C% các chất có trong X

Những câu hỏi liên quan
Dẫn luồng khí H2 (dư) đi qua ống sứ đựng 25,6 gam hỗn hợp X gồm Fe3O4, MgO, CuO nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được 20,8 gam chất rắn. Mặt khác, 0,15 mol hỗn hợp X tác dụng vừa đủ với 225 ml dung dịch HCl 2M. Viết c ác phương trình phản ứng xảy ra và tính phần trăm số mol của mỗi chất trong hỗn hợp X
Dẫn lượng dư khí CO đi qua 25,6 (g) hỗn hợp X gồm Fe3O4, MgO, CuO nung nóng đến khi các phản ứng xảy ra hoàn toàn thu được 20,8 (g) chất rắn. Mặt khác, để hòa tan hết 0,15 mol hỗn hợp X cần dùng vừa đủ 450ml dung dịch HCl 1M. Viết các PTHH xảy ra và tính thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp X.
Đặt: nFe3O4= x mol
nMgO = y mol
nCuO= z mol
mX= 232x + 40y + 80z = 25.6g (1)
Fe3O4 + 4CO -to-> 3Fe + 4CO2
x________________3x
CuO + CO -to-> Cu + CO2
z_____________z
mCr= mFe + mMgO + mCu= 3x*56 + 40y + 64z = 20.8 g
<=> 168x + 40y + 64z = 20.8 (2)
Ta có :
Trong 0.15 mol hh có :
kx (mol) Fe3O4, ky (mol) MgO , kx (mol) CuO
nHCl= 0.45*1=0.45 mol
Fe3O4 + 8HCl --> FeCl2 + 2FeCl3 + 4H2O
kx______8kx
MgO + 2HCl --> MgCl2 + H2O
ky______2ky
CuO + 2HCl --> CuCl2 + H2O
kz______2kz
nHCl= 8kx + 2ky + 2kz = 0.45
<=> k(8x + 2y + 2z) = 0.45 (3)
nhh= k( x + y+ z ) = 0.15 (4)
Lấy (3) chia (4) :
(8x + 2y + 2z)/ (x+y+z) = 0.45/0.15=3
<=> 8x + 2y + 2z = 3x + 3y + 3z
<=> 5x -y - z = 0 (5)
Giải (1), (2) và (5) :
x= 0.05
y= 0.15
z=0.1
mFe3O4= 0.05*232=11.6g
mMgO= 0.15*40=6g
mCuO= 0.1*80=8g
%Fe3O4= 45.3125%
%MgO= 23.4375%
%CuO= 31.25%
Đúng 3
Bình luận (0)
Dẫn luồng CO dư đi qua 37.68 g hỗn hợp X gồm : CuO; MgO;PbO ;Fe3O4 , nung hỗn hợp đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp chất rắn Y và hỗn hợp khí Z . Sục hỗn hợp khí Z vào dung dịch Ca(OH)2 dư thu được 34 gam kết tủa trắng . Xác định khối lượng của hỗn hợp chất rắn Y?
CO + X -> Y + Khí Z gồm CO2 và CO
khí Z + Ca(OH )2 -> kết tủa trắng : CaCO3
=> chất khí phản ứng với Ca(OH)2 tạo kết tủa là CO2
m ( CaCO3) = 34 g; M (CaCO3)=40+12+16x3=100 (đvc)
=> n ( CaCO3) = 34:100=0,34 ( mol)
=> n( CO2) = n ( C) trong CO2 = n (C) trong CaCO3 =n ( CaCO3) =0,34 (mol)
=> n ( CO) phản ứng = n ( C) trong CO phản ứng = n ( C) trong CO2 tạo ra =n ( CO2) tạo ra =0, 34 (mol)
=> m( CO ) phản ứng =0, 34. (12+16)=9,52 g
m ( CO2) tạo ra =0,34. (12+16.2)=14,96 g
Áp dụng định luật bảo toàn khối lượng:
m (CO ) pứng + m (X) = m( CO2) tạo ra + m( Y)
=> 9,52 +37,68= 14,96 +m(Y)
=> m( Y) =32,24 g
Vậy khối lượng của Y là 32, 24 g
Đúng 0
Bình luận (0)
Cho luồng khí H2 dư đi qua hỗn hợp X gồm Fe3O4 và CuO nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được 29,6 gam chất rắn. Mặt khác, để hòa tan hết lượng X trên cần vừa đủ 600 ml dung dịch HCl 2M. Tính phần trăm khối lượng mỗi chất trong X
2H(Axit) + O(Oxit) → H2O
→ nH(Axit) = 2.nO(Oxit)
Gọi số mol của Fe3O4 và CuO lần lượt là x và y
BTNT O: 4x + y = 0,6
BTKL: 56 . 3x + 64y = 29,6
=> x = 0,1 và y = 0,2
=> %Fe3O4 = 59,18%
%CuO = 40,82%
Đúng 0
Bình luận (0)
Dẫn h2 dư qua 25,6 gam hhX gồm Fe3O4 MgO, CuO nung nóng cho đến khi phản ứng xảy ra hoàn toàn sau phản ứng thu đc 20,8 gam chất khí. Mặc khác cho 0,15 mol hhX tác dụng vừa đủ với 225 ml dd HCl 1M . Tính % khối lượng các chất trong X
Cho hỗn hợp X gồm
A
l
2
O
3
,
M
g
O
,
F
e
3
O
4
, CuO vào dung dịch NaOH dư còn lại chất rắn không tan Y. Cho luồng khí CO dư đi qua Y thu được chất rắn Z. Giả sử các phản ứng xảy ra hoàn toàn, Z gồm A.
M
g
O
,
F
e...
Đọc tiếp
Cho hỗn hợp X gồm A l 2 O 3 , M g O , F e 3 O 4 , CuO vào dung dịch NaOH dư còn lại chất rắn không tan Y. Cho luồng khí CO dư đi qua Y thu được chất rắn Z. Giả sử các phản ứng xảy ra hoàn toàn, Z gồm
A. M g O , F e , C u
B. M g , F e , C u
C. M g O , F e 3 O 4 , C u
D. M g , A l , F e , C u
Cho khí CO dư đi qua hỗn hợp gồm Fe3O4, MgO, CuO, FeO, Al2O3 (nung nóng). Khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm A. MgO, Al2O3, Fe3O4, Cu B. MgO, Al2O3, Fe2O3, Fe, Cu C. MgO, Al2O3, Fe, Cu D. Mg, Al, Fe, Cu
Đọc tiếp
Cho khí CO dư đi qua hỗn hợp gồm Fe3O4, MgO, CuO, FeO, Al2O3 (nung nóng). Khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm
A. MgO, Al2O3, Fe3O4, Cu
B. MgO, Al2O3, Fe2O3, Fe, Cu
C. MgO, Al2O3, Fe, Cu
D. Mg, Al, Fe, Cu
Dẫn luồng khí H2 (dư) đi qua ống sứ đựng 30,72 gam hỗn hợp (X) gồm Fe3O4, MgO và CuO nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được 24,96 gam chất rắn. Mặt khác 0,18 mol hỗn hợp (X) tác dụng vừa đủ với 270 ml dung dịch HCl 2M . Viết phương trình hóa học của các phản ứng xảy ra và tính phần trăm số mol của mỗi chất trong hỗn hợp (X).
PTHH: Fe3O4+4H2\(\underrightarrow{t^O}\)3Fe+4H2O
a 3a
CuO+H2\(\underrightarrow{t^O}\)Cu+H2O
c c
Fe3O4+8HCl\(\rightarrow\)FeCl2+2FeCl3+4H2O
ka 8ka
MgO+2HCl\(\rightarrow\)MgCl2+H2O
kb 2kb
CuO+2HCl\(\rightarrow\)CuCl2+H2O
kc 2kc
Đặt a,b,c lần lượt là số mol của Fe3O4, MgO,CuO trong 30,72 g X(a,b,c>0)\(\Rightarrow\)232a+40b+80c=30,72(1)
168a+40b+64c=24,96(2)
Đặt k là tỉ lề số phần mỗi chất trong 30,72 g X so với 0,18 mol X
\(\Rightarrow\)ka,kb,kc lần lượt là số mol của Fe3O4, MgO, CuO trong 0,18mol X
\(\Rightarrow\)ka+kb+kc=0,18(3)
Ta có:nHCl=0,54(mol)\(\Rightarrow\)8ka+2kb+2kc=0,54(4)
Từ (3) và (4), suy ra:-5a+b+c=0(5)
Từ(1), (2), (5), suy ra:a=0,06;b=0,18;c=0,12
Vậy:%nFe3O4=0,06:(0,06+0,18+0,12).100%=16,67%
%nMgO=0,18:(0,06+0,18+0,12)=50%
%nCuO=100%-16,67%-50%=33,33%
Đúng 0
Bình luận (0)
Một hỗn hợp A gồm các oxit MgO, CuO, Fe2O3. Fe có khối lượng bằng m. Dẫn luồng khí CO dư đi qua A nung nóng đến khi phản ứng xảy ra hoàn toàn thu được chất rắn B có khối lượng là 6,8g và hỗn hợp khí C. Cho C vào dung dịch Ca(OH)2 dư thì xảy ra phản ứng. Sau phản ứng thu được 20 gam kết tủa. Tìm m
\(Ca(OH)_2 + CO_2 \to CaCO_3 + H_2O\\ n_{CO_2} = n_{CaCO_3} = \dfrac{20}{100} = 0,2(mol)\\ CO + O_{oxit} \to CO_2\\ n_{O(oxit)} = n_{CO_2} = 0,2(mol)\\ \Rightarrow m = m_B + m_{O(pư)} = 6,8 + 0,2.16 = 10(gam)\)
Đúng 1
Bình luận (0)